SPPIN - Saints-Pères Paris Institute for the Neurosciences - CNRS UMR 8003
Université Paris Cité
F-75006 Paris
France
Dr. Ahmed Hamraoui
Team 3 - Biology and physiopathology of the spinal cord
+33 1 76 53 43 41 (switchboard)
Student :
Nouvel article « Les neurones sont élastiques… » ( article HAL, annonce INSP )
Mes projets
- Propriétés mécaniques des neurones
- Physique de la croissance axonale
- Surfaces autonettoyantes
- Innovations contre les Infections Périprothétiques
- Transferts vers l’industrie
La régénérescence du système nerveux central et périphérique, suite à une pathologie ou un traumatisme, est un enjeu sociétal majeur dans un contexte de vieillissement de la population. Cette plasticité pilotée par la croissance et la différenciation des cellules en neurones par exemple dépend de bons nombres de paramètres. La corrélation entre ces mécanismes de réparation et la réponse élastique de l’environnement et des cellules elles-mêmes est souvent évoquée mais reste encore à ce jour difficilement quantifiable. Néanmoins, des chercheurs de l’INSP en collaboration avec le LCMCP et SPPIN ont franchi une étape cruciale vers cet objectif en quantifiant, à l’échelle micrométrique, les inhomogénéités élastiques au cœur même du neurone.
Boostez et orienter la régénération nerveuse : Un regard sur la croissance axonale
Pour élaborer les circuits neuronaux, les axones doivent interpréter divers signaux de guidage, générés à différentes étapes et localisations, afin de se diriger vers leurs cibles. Comprendre ces interactions ouvrirait la voie à l’utilisation de biomatériaux novateurs pour restaurer la fonction en cas de lésions. Ce projet se concentre spécifiquement sur la réparation des axones des motoneurones suite à des traumatismes graves. Une caractéristique distinctive du système nerveux périphérique réside dans la longueur de ses axones, rendant leur régénération lente et inefficace. Ainsi, il est crucial de développer des mécanismes de régénération accélérée, ce qui exige une compréhension approfondie des interactions neuronales avec leur environnement.
Bien qu’il existe des solutions novatrices pour stimuler la réparation nerveuse, les mécanismes exacts de la régénération neuronale restent mal compris. De plus, mon projet explore l’utilisation du champ électrique pour accélérer la régénération, une approche prometteuse mais largement sous-exploitée.
Stratégies expérimentales pour stimuler la croissance axonale
Nous avons étudié la stimulation, sans NGF, de la croissance axonale sur des surfaces qui combinent une nano-structuration physique à laquelle sont associés des gradients locaux de l’énergie d’adhésion [PMID : 19419846 ; PMID : 20149439].
Système étudié et préparation de la surface : exemple
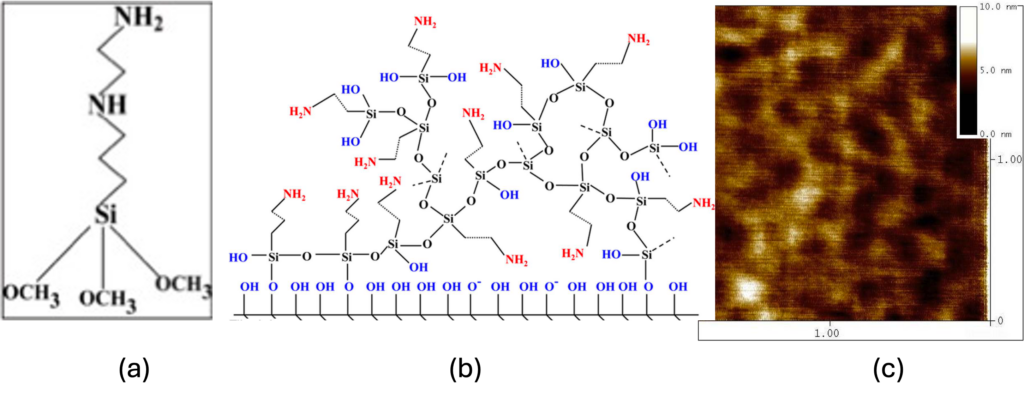
Les substrats utilisés sont des lamelles de verre dont la surface est préalablement traitée par chimisorption d’amino-silane : C8H22N2O3Si (EDA pour Ethyl-Di-Amine, voir figure 1a). Pour assurer une surface propre, celles-ci subissent un dégraissage dans deux bains successifs de chloroforme, agités par ultrasons pendant 20 minutes. Ensuite, le substrat est immergé dans un mélange d’eau oxygénée et d’acide sulfurique dans un rapport 3/7 v :v, suivi d’un rinçage à l’eau distillée et d’un séchage sous flux d’azote.
La silanisation est réalisée en plongeant la surface propre dans une solution composée de méthanol (94%), d’acide acétique (1mM), d’eau (4%) et d’EDA (2%), pour une durée déterminée selon les expériences. Après cette étape, les surfaces sont rincées au méthanol et séchées sous un flux d’azote. Elles peuvent ensuite être stockées et aseptisées dans le méthanol. La figure 1b illustre le schéma de la molécule EDA polycondensée sur la surface de verre hydroxylée, tandis que la figure 1c présente une image de la topographie de la surface verre-EDA obtenue par AFM en mode tapping.
Exemples de Résultats et discussion :
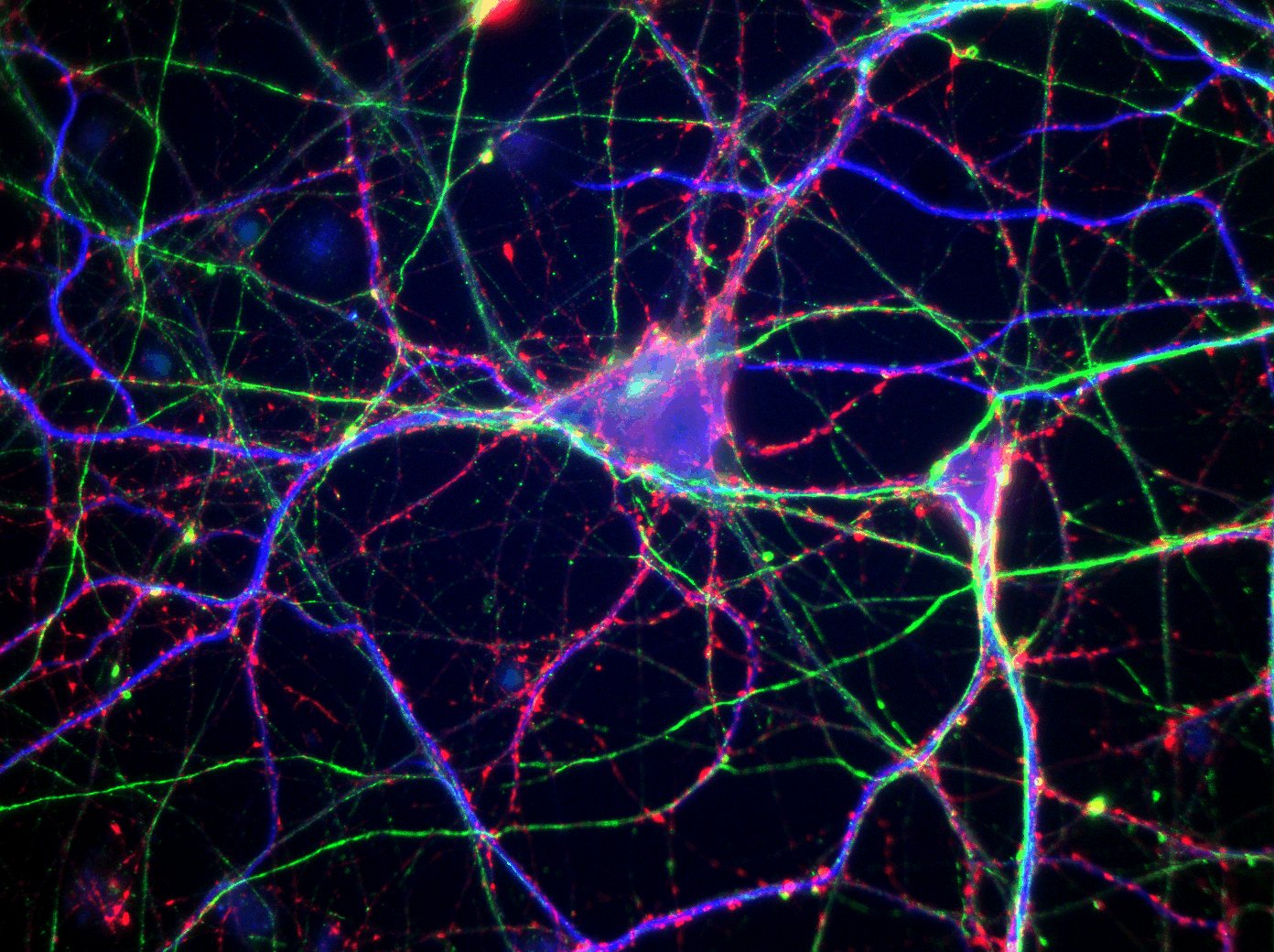
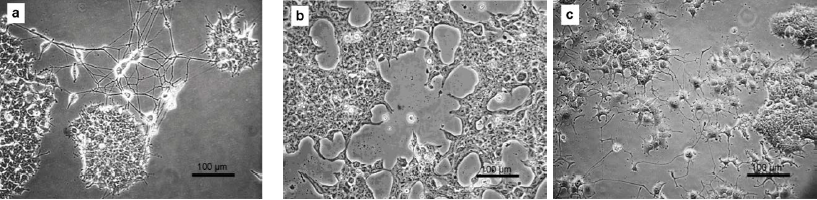
La figure 2 représente trois photographies de réseaux de neurites formées après 5 jours de culture de PC12 sur des surfaces verre-EDA et sans NGF (fig. 2a, la figure 2c montre des PC12 cultivées sur PLL en présence de NGF dans le milieu de culture (pour le protocole en détail voir les références [PMID : 19419846 ; PMID : 20149439] ). Il est évident que la présence des gradients locaux dans l’énergie d’adhésion ont un effet significatif sur la genèse des neurites et probablement sur leur vitesse de croissance.
15 cm de diamètre (5,6 105 cm−2 environ).
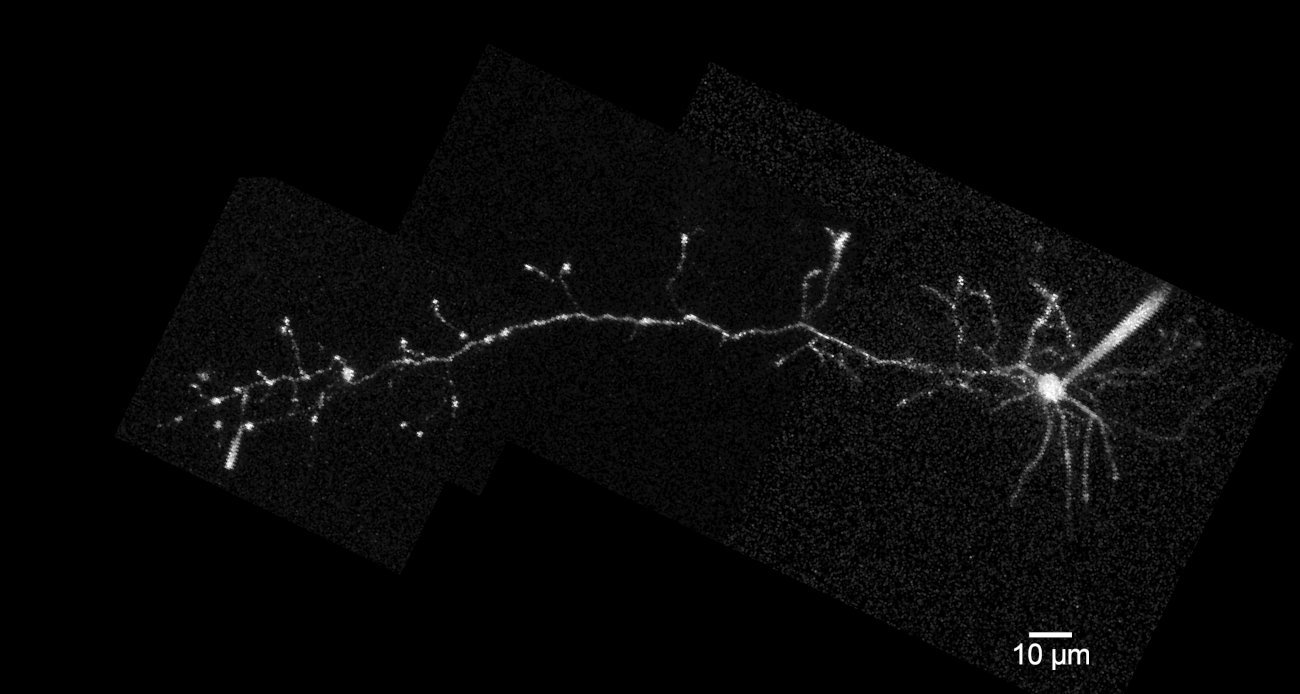
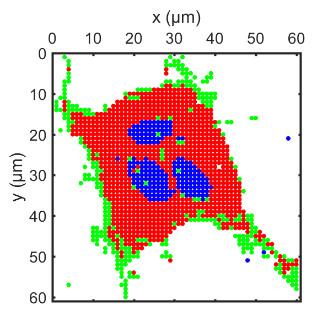
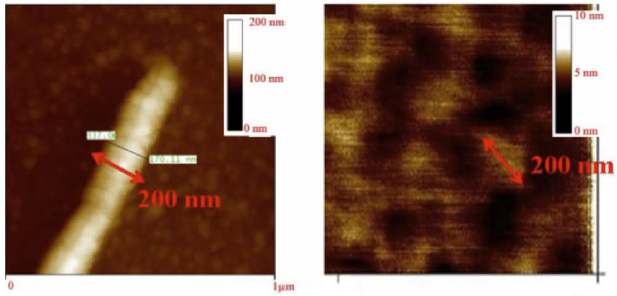
En utilisant une méthode simple de fixation des cellules avec du glutaraldéhyde à 2% (v/v) dans le milieu de culture, nous avons réussi à visualiser des cônes de croissance à l’aide du microscope à force atomique (AFM). La Figure 3 illustre un cône de croissance d’un neurone PC12, offrant une représentation des variations de hauteur. Cette image fournit des informations précieuses : elle indique initialement une hauteur d’environ 4 μm pour une neurite à son extrémité, avec une largeur d’environ 1 μm. Il est important de noter que les filopodes ne sont pas exclusivement situés à l’extrémité du cône, mais sont répartis tout autour de celui-ci de manière relativement uniforme dans toutes les directions. La figure 4 illustre la topographie d’un filopode, dont les dimensions mesurées sont d’environ 200 nm de largeur et 40 nm de hauteur. Cela suggère que le filopode peut réagir aux gradients locaux dans l’énergie d’adhésion.

2%v : v dans le milieu de culture.
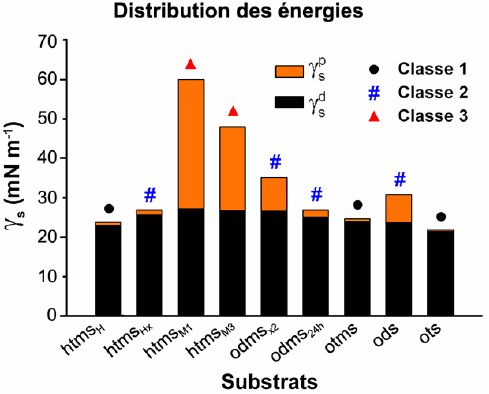
Un exemple supplémentaire illustrant la confirmation de notre hypothèse sur l’importance du gradient dans l’énergie d’adhésion dans la neuritogenèse est présenté dans la figure 5. Cette figure met en évidence des cellules PC12 cultivées sur trois surfaces distinctes, chacune modifiée par des molécules terminées par un groupe −CH3. Ces surfaces ont été caractérisées à l’aide de spectroscopie de génération de fréquence-somme (SFG). La SFG permet de distinguer la classe 1 des classes 2 et 3, ces dernières se distinguant par des distributions différentes de la composante
non-dispersive (γp) de l’énergie de surface, comme le montre la figure 6. Les figures 5 et 6 mettent
également en évidence une corrélation significative entre l’ordre surfacique, la distribution des
composantes dispersives γd et non-dispersives γp des énergies de surface des substrats, d’une
part, et l’adhésion et la différenciation des cellules PC12, d’autre part. Les trois classes de surfaces sont les suivantes :
- Classe 1 : OTS (Octadécyltrichlorosilane)
- Classe 2 : ODMS (Octadécyldiméthylméthoxysilane)
- Classe 3 : HTMS (n-Hexyltriméthoxysilane)

Innovations Contre la Poussière: Des Panneaux Solaires plus Performants sur Terre et dans l’Espace
L’accumulation de poussière sur les panneaux solaires constitue un véritable problème, comme le montre l’exemple du Sahara où le sable s’amasse en grande quantité. Cependant, diverses solutions sont en cours d’étude, notamment le nettoyage électrostatique, qui consiste à charger les particules de poussière pour les éliminer par effet électrostatique. Ce sujet est également applicable au domaine spatial, où la poussière et les particules peuvent affecter les performances des panneaux solaires sur les engins spatiaux. L’objectif est de caractériser les propriétés superficielles et la structure du matériau en utilisant différentes techniques disponibles au laboratoire, parmi lesquelles les mesures d’angle de contact sont particulièrement importantes.
Je participe à ce projet en tant que responsable des programmes de prématuration avec la SATT-Lutech et du programme TOUBKAL2024 en partenariat avec le Maroc.
Vers des Implants plus Sûrs: Innovations contre les Infections Articulaires Périprothétiques
Dans le cadre du programme de prématuration avec la SATT-Lutech et de la collaboration avec la Fédération Hospitalo Universitaire PROTHEE, je suis impliqué dans l’élaboration d’un dispositif implantable aux propriétés dynamiques de sa surface. L’augmentation de l’espérance de vie et de la qualité de vie, ainsi que les exigences fonctionnelles élevées de la population âgée, expliquent la hausse des procédures impliquant l’implantation de biomatériaux.
Entre 2005 et 2030, la demande d’arthroplasties totales de la hanche devrait augmenter de 174 %, atteignant 572 000 procédures, et celle des arthroplasties du genou de 673 %, atteignant 3,48 millions de procédures aux États-Unis. Comme 1 à 2 % des arthroplasties entraînent une infection, l’incidence des infections articulaires périprothétiques (IAP) augmentera avec le temps. Bien que ces infections soient rares, elles sont difficiles à prévenir, diagnostiquer et guérir, nécessitant souvent des opérations multiples, des hospitalisations prolongées, des réadmissions fréquentes et l’utilisation prolongée d’antibiotiques et d’analgésiques. L’IAP est donc l’une des complications chirurgicales les plus complexes et graves, tant pour les patients que pour les chirurgiens et le système de santé. Elle est aussi une cause majeure de procès en raison des séquelles pour les patients. Le coût annuel des réopérations pour infection dans les hôpitaux américains est passé de 320 millions de dollars à 566 millions de dollars entre 2001 et 2009.
L’arthroplastie, reflétant le vieillissement de la population, est une procédure de plus en plus courante. En France, plus de 200 000 arthroplasties sont réalisées chaque année, entraînant plus de 3 000 infections articulaires prothétiques (IAP) ; le taux d’incidence (1,5 %) augmente avec l’accroissement des comorbidités des patients. Ces infections, difficiles à prévenir, diagnostiquer et guérir, nécessitent souvent des opérations multiples, des hospitalisations prolongées et l’utilisation prolongée d’antibiotiques, entraînant un impact physique et psychosocial significatif pour les patients et des coûts élevés pour le système de santé. Malgré les avancées du Centre de Référence des Infections Ostéo-Articulaires Complexes (CRIOAC), les IAP restent peu explorées par la recherche, y compris dans les domaines de la pathologie osseuse et des biomatériaux.
La prévention des IAP repose sur deux méthodes innovantes développées par des équipes de recherche : un biomatériau à surface modifiée inhibant l’adhésion bactérienne et un dispositif implantable pour nettoyer la surface des biomatériaux/prothèses. Le diagnostic microbiologique des IAP utilise de nouvelles techniques, notamment la métagénomique, en exploitant l’équipement existant pour l’identification virale à l’hôpital Saint-Louis.
Unilever (Hollande) :
Mouillabilité des poudres en fonction de la viscosité et de la température du liquide
Dans le cadre de ce contrat, j’ai étudié l’influence du transfert thermique sur le mouillage pour résoudre des problèmes rencontrés dans la production de tablettes de lessive. L’étude s’est concentrée sur les effets de la différence de température entre le liquide et le substrat sur le processus de mouillage. Pour des raisons de confidentialité, je ne peux pas fournir plus de détails sur ce travail.
Glaverbel (Belgique) :
Traitement du verre et dépôt de couches d’argenture
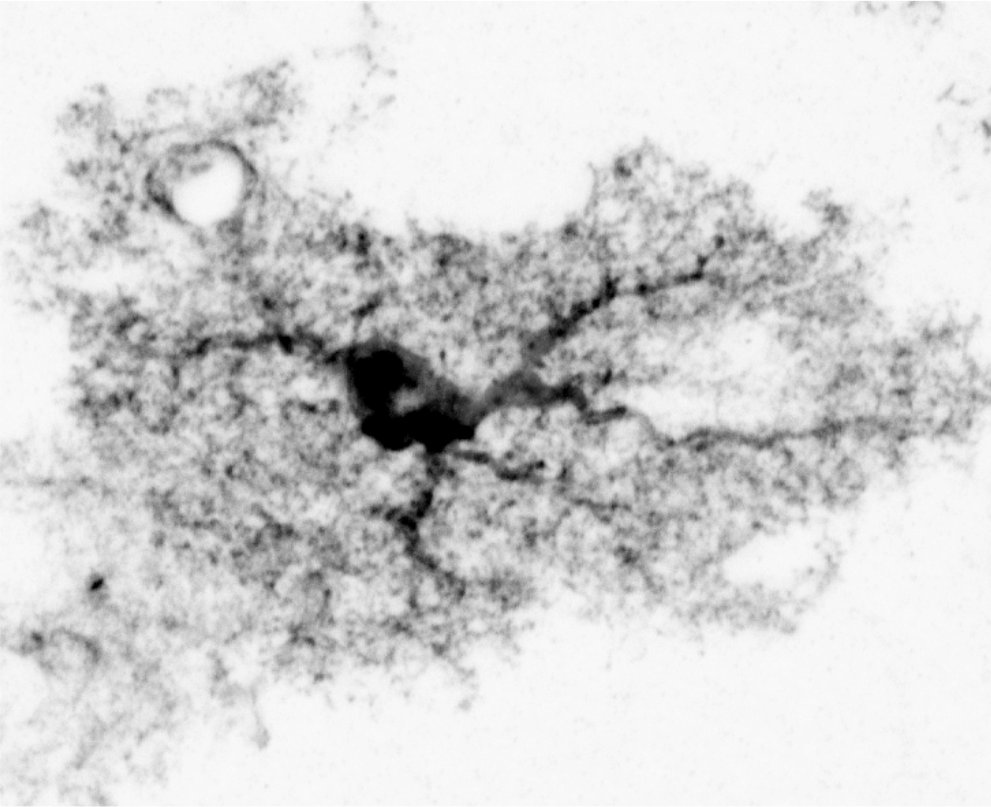
Dans le cadre du programme First-Europe, j’ai travaillé au centre de recherche et développement de Glaverbel à Jumet (Belgique) ainsi que dans l’unité de production des miroirs à Zeebrugge (Belgique). Mon travail consistait à résoudre un problème de qualité des miroirs, qui présentaient une anomalie appelée “voile”, caractérisée par l’apparition de zones claires et sombres. Cette anomalie était attribuée à des variations d’épaisseur de la couche d’argent. Pour comprendre la formation et l’origine de cette variation d’épaisseur, il a fallu reproduire sous microscope la réaction d’oxydoréduction responsable de la formation de la couche d’argent (voir figure).

(a) Cristaux en formation dans la solution réductrice et apparition des zones d’argent épaisses après le passage du front de la solution d’argenture (flèche rouge). (b) On observe l’apparition des zones d’argenture épaisses (flèches) autour des cristaux de la solution réductrice.
(c) Image de la couche d’argent déposée après filtration de la solution réductrice. On remarque que l’épaisseur de la couche est uniforme, et le miroir ne présente plus d’anomalie. (La tache noire au centre correspond à l’endroit du dépôt des deux solutions : argent et réducteur).
Arjo Wiggins (Belgique) : Fabrication du papier
Caractérisation du papier et optimisation des performances selon l’utilisation : écriture à main, impression, papiers pour facturations
Objectif de l’étude
Cette étude visait à relier les propriétés de mouillage des fibres constituant le papier aux propriétés de mouillage de sa surface. Pour ce faire, nous avons réalisé des expériences de cinétique d’imbibition en accrochant un échantillon de papier à une balance tensiométrique et des expériences de dynamique de mouillage en étudiant la relaxation de gouttes d’eau et d’encre sur la surface du papier. Cependant, nous n’avons pas pu établir de relation directe entre les propriétés de mouillage de la surface du papier et celles de ses fibres.
Libeltex (Belgique) :
Mouillage des fibres, et des tissus textiles
Étude des tissus produits par LibelTex pour une utilisation optimale dans les couches-culottes
J’ai été chargé par le Centre de Recherche en Modélisation Moléculaire (CRMM) qui fait partie du laboratoire Centre d’Excellence Materia Nova d’étudier les tissus produits par LibelTex afin de déterminer la densité optimale pour leur utilisation dans les couches-culottes. Pour ce faire, j’ai mené des investigations en utilisant une balance tensiométrique pour mesurer la quantité d’eau absorbée par le tissu. L’analyse des résultats s’est basée sur le modèle de Lucas-Washburn. Cette méthode a permis de démontrer l’existence d’un extremum du rayon effectif correspondant à une densité inférieure à celle habituellement produite par LibelTex (voir figure).
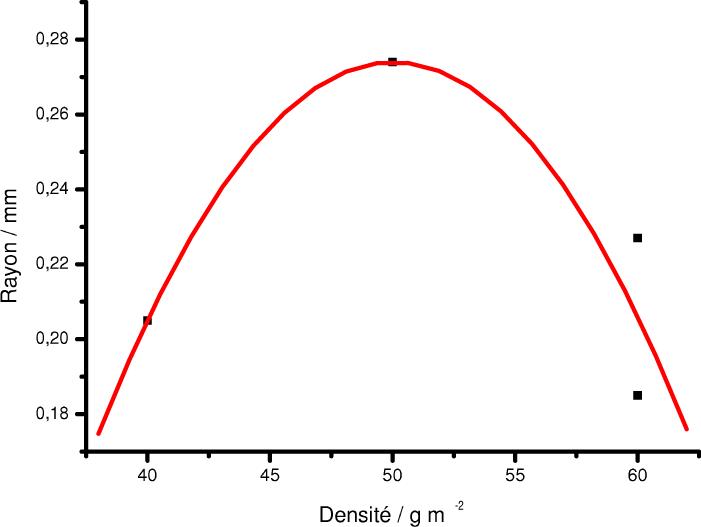
Rayon effectif moyen en fonction de la densité du tissu
Recent Publications
Articles
- Decoding Wetting Behavior: Capillary Rise Experiments with Amphiphilic Compounds and Theoretical Aspects
Hamraoui A, Thuresson K, Nylander T : Langmuir, 2025 - Decoding wetting behavior: capillary rise experiments with amphiphilic compounds and theoretical aspects
Ahmed Hamraoui, Krister Thuresson, Tommy Nylander : Langmuir, 2025 - Cell adhesion and surface interactions: A comprehensive review of surface energy, wettability, and topography effects
Hamraoui A : AIP Advances, 2025 - Managing surface energy dynamics for enhanced axonal growth: An overview of present and future challenges
Sénépart O, Legay C, Hamraoui A : Biophysics Reviews, 2025 - Ice templating water-stable macroporous polysaccharide hydrogels to mimic plant stems.
Komiyama K, Allard M, Eschenbrenner C, Sicard C, Hamraoui A, Fernandes F : Journal of Materials Chemistry B, 2025 - Contributions of Surface and Interface Physical Chemistry to Biology
Ahmed Hamraoui : (preprint), 2024 - Complementarity between Brillouin signature and Scholte wave for controlled elasticity in fibrillated collagen medium for culture cell
Ahmed Hamraoui, Océane Sénépart, Laurent Belliard : Applied Physics Letters, 2024 - Data clustering analysis of scanning ultrafast acoustic experiments. How acoustic and structural properties of a motoneuron are revealed
Péronne E, Sénépart O, Legay C, Semprez F, Hamraoui A, Belliard L : {Physical Review Applied}, 2022 - Adhesion energy modulation acts as an NGF receptor activator for neuronal differentiation in NGF-free medium
Sénépart O, Legay C, Hélary C, Hamraoui A : Advanced Materials Interfaces, 2022 - Correlative Imaging of Motoneuronal Cell Elasticity by Pump and Probe Spectroscopy.
Hamraoui A, Sénépart O, Schneider M, Malaquin S, Péronne E, Becerra L, Semprez F, Legay C, Belliard L : Biophys J, 2021 - Picosecond ultrasounds as elasticity probes in neuron-like cells models
Viel A, Péronne E, Sénépart O, Becerra L, Legay C, Semprez F, Trichet L, Coradin T, Hamraoui A, Belliard L : Applied Physics Letters, 2019 - Ice-templating beet-root pectin foams: Controlling texture, mechanics and capillary properties
Sarah Christoph, Ahmed Hamraoui, Estelle Bonnin, Catherine Garnier, Thibaud Coradin, Francisco M Fernandes : Chemical Engineering Journal, 2018 - Surface-induced assembly of sophorolipids.
Peyre J, Hamraoui A, Faustini M, Humblot V, Baccile N : Phys Chem Chem Phys, 2017 - Substrate-induced PC12 cell differentiation without filopodial, lamellipodial activity or NGF stimulationa.
Lamour G, Souès S, Hamraoui A : Macromol Biosci, 2015 - Tuning surface energy at the nanometer scale: A new step towards controlling neuronal differentiation?
Lamour G, Souès S, Collart E, Colline S, Bardoue N, Hamraoui A : Journal of Nanoscience Letters, 2013 - Neuritogenesis on antagonist surfaces
Lamour G, Souès S, Hamraoui A : Global Journal of Physical Chemistry| Volume, 2011 - Interplay between long- and short-range interactions drives neuritogenesis on stiff surfaces.
Lamour G, Souès S, Hamraoui A : J Biomed Mater Res A, 2011 - Contact angle measurements using a simplified experimental setup
Lamour G, Hamraoui A, Buvailo A, Xing Y, Keuleyan S, Prakash V, Eftekhari-Bafrooei A, Borguet E : Journal of chemical education, 2010 - Neuronal adhesion and differentiation driven by nanoscale surface free-energy gradients.
Lamour G, Eftekhari-Bafrooei A, Borguet E, Souès S, Hamraoui A : Biomaterials, 2010 - Influence of surface energy distribution on neuritogenesis.
Lamour G, Journiac N, Souès S, Bonneau S, Nassoy P, Hamraoui A : Colloids Surf B Biointerfaces, 2009 - Layering and prewetting in experimental systems: an assessment cross-referred to current theories.
Hamraoui A, Privat M : Adv Colloid Interface Sci, 2009 - Modelling photochemical reactions in atmospheric water droplets: An assessment of the importance of surface processes
Davide Vione, Claudio Minero, Ahmed Hamraoui, Mireille Privat : Atmospheric Environment, 2007 - Fingering phenomena during spreading of surfactant solutions
Hamraoui A, Cachile M, Poulard C, Cazabat A : Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2004 - Films driven by surface tension gradients.
Cachile M, Schneemilch M, Hamraoui A, Cazabat AM : Adv Colloid Interface Sci, 2002 - Analytical approach for the Lucas-Washburn equation.
Hamraoui A, Nylander T : J Colloid Interface Sci, 2002 - Critical and wetting transitional adsorption behaviour in a liquid system against vapour and other walls
Huruguen J, Amara M, Méar A, Hamraoui H, Olier R, Privat M : Journal of Physics: Condensed Matter, 2001 - Can a dynamic contact angle be understood in terms of a friction coefficient?
Hamraoui A, Thuresson K, Nylander T, Yaminsky V : Journal of colloid and interface science, 2000 - Interfacial properties of whey proteins at air/water and oil/water interfaces studied by dynamic drop tensiometry, ellipsometry and spreading kinetics
Nylander T, Hamraoui A, Paulsson M : International journal of food science \& technology, 1999 - Surface phase transitions at liquid-mixture/solid interfaces
Mazeas I, P{\’e}lerin P, Sellami H, Hamraoui A, Olier R, Privat M : Langmuir, 1999 - Impact of Bulk Phase Transitions and Wetting Transitions on Adsorption Isotherms in Binary Systems in Contact with Solid.
Hamraoui A, Privat M : J Colloid Interface Sci, 1998 - Experimental Evidence of Pure Layering at the Solid/Liquid Binary Mixture Interface. Silica/Water- 2, 5-Dimethylpyridine System
Sellami H, Hamraoui A, Privat M, Olier R : Langmuir, 1998 - Layering in a two-component liquid system undergoing a phase separation
Hamraoui A, Privat M, Sellami H : The Journal of chemical physics, 1997 - Prewetting transition influenced by layeringlike transitions at a binary liquid/solid interface
Hamraoui A, Privat M : The Journal of chemical physics, 1997 - Monolayers, critical layers and wetting films in a liquid-liquid-solid system undergoing a wetting transition. Experimental study
Privat M, Amara M, Hamraoui A, Sellami H, Mear A : Berichte der Bunsengesellschaft f{\, 1994
Chapter
- Dynamic wetting and dewetting by aqueous solutions containing amphiphilic compounds
Hamraoui Ahmed, Thuresson Krister, Nylander Tommy, Eskilsson Krister, Yaminsky Vassili : extracted from Surface and Colloid Science Valdemaras Razumas, Björn Lindman, Tommy Nylander - Springer, pages 113-119, ISBN:978-3-540-44941-6, 2001
Speech communications / proceedings
- Extracting Weak Signal with the Help of Data Clustering: Application to Motoneuron Adhesion
Emmanuel Péronne, Sophie Malaquin, Loic Becerra, Laurent Belliard, Ahmed Hamraoui, Claire Legay, Fannie Semprez : Forum Acusticum, Lyon, France, 2020 - Picosecond ultrasounds as elasticity probes in neuron-like cells models.
Laurent Belliard, Alexis Viel, Emmanuel Péronne, Océane Sénépart, Loic Becerra, Claire Legay, Fannie Semprez, Lea Trichet, Thibaud Coradin, Ahmed Hamraoui : Forum Acusticum, Lyon, France, 2020
Patents
- la pré-stimulation électrique d’un dispositif implantable pour la réparation du nerf
Ahmed HAMRAOUI, Océane SENEPART, Claire LEGAY, Hafsa ER-ROUASSI, Richard Junior AMEDZROVI AGBESI : Patent # : DSO2025028091, 2025 - Nerve repair implant: International application
A Hamraoui, O Sénépart, C Legay : Patent # : WO2024/241069, 2024